Ces scientifiques de l’Université de Californie – San Diego viennent de décrypter précisément, à l’aide d’un assembloïde en 3D, comment le virus SRAS-CoV-2 responsable du COVID-19 se propage dans les vaisseaux sanguins pour infecter les péricytes (cellules situées près de l’endothélium des vaisseaux sanguins), qui amplifient l'infection et propagent l'infection à d'autres types de cellules dans le cerveau. Cette recherche expérimentale, publiée dans la revue Nature Medicine contredit un certain nombre d’études qui limitaient les effets du virus sur le cerveau à une inflammation et des lésions, mais excluaient l’infection du cerveau. Certaines cellules autres que les neurones semblent pourtant jouer le rôle de cheval de Troie.
« Certaines observations cliniques et épidémiologiques suggèrent que le cerveau peut être impliqué dans l'infection par le SRAS-CoV-2 », rectifie l'auteur principal, le Dr Joseph Gleeson, professeur de neurosciences et directeur de recherche en neurosciences pour la médecine génomique à l'UC San Diego. « La perspective de lésions cérébrales induites par COVID-19 est devenue une préoccupation majeure dans les cas de COVID long, mais les neurones humains en culture ne semblent pas sensibles à l'infection. Des publications antérieures suggèrent que les cellules qui fabriquent le liquide céphalo-rachidien pourraient être infectées par le SRAS- CoV-2, mais il nous a semblé qu’il existait d'autres voies d'entrée possibles ».
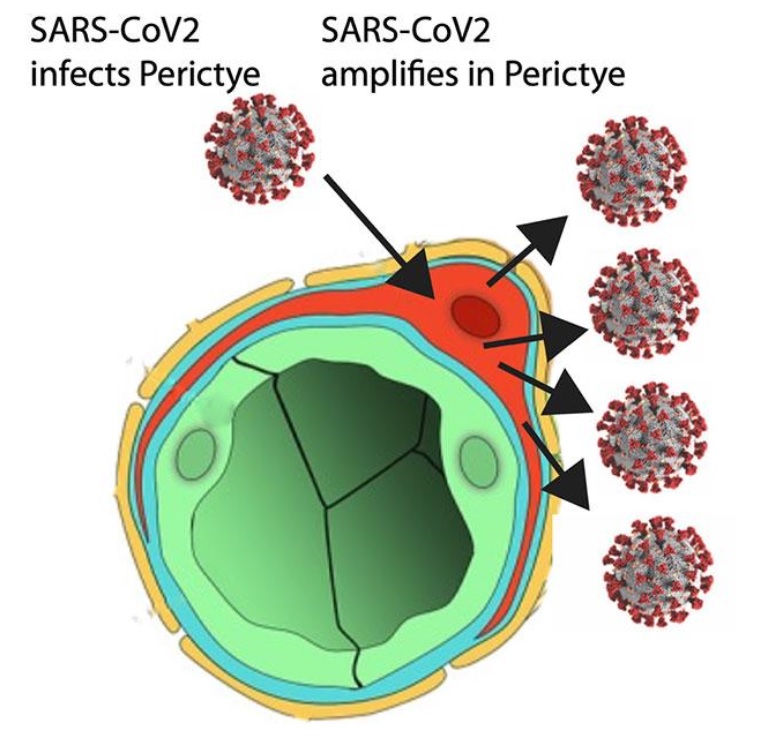
Ainsi, le modèle développé par les scientifiques, un « assembloïde » un modèle à base de cellules souches, révèle (voir visuel) une voie d'entrée possible du virus, via les vaisseaux sanguins (en vert) et précisément les péricytes (en rouge).
Les neurones sont résistants à l'infection par le SRAS-CoV-2 mais pas les péricytes
L’équipe confirme avec ce modèle que les cellules neurales humaines sont résistantes à l'infection par le SRAS-CoV-2 mais que les péricytes, des cellules spécialisées qui s'enroulent autour des vaisseaux sanguins et portent le récepteur du SRAS-CoV2 pourraient propager l’infection : les chercheurs ont introduit des péricytes dans des cultures de cellules neurales tridimensionnelles –
des organoïdes cérébraux – pour créer des « assembloïdes »,
un modèle de cellules souches sophistiqué qui comportait de nombreux types de cellules cérébrales en plus des péricytes et présentaient une infection robuste par le SRAS-CoV-2.
Quel processus possible ? Le coronavirus « a pu » infecter les péricytes, qui ont servi d'usines localisées pour la production de SARS-CoV-2. Ces SARS-CoV-2 produits localement ont pu ensuite se propager à d'autres types de cellules, entraînant des dommages plus étendus. Les chercheurs constatent notamment que les cellules de soutien appelées astrocytes sont la cible principale de cette infection secondaire.
Il existe donc bien une voire d’infection possible du cerveau, qui passe par les vaisseaux sanguins, où le SRAS-CoV-2 peut infecter les péricytes, puis se propager à d'autres types de cellules du cerveau. Les péricytes infectés peuvent également entraîner une inflammation des vaisseaux sanguins, suivie d'une coagulation, d'un accident vasculaire cérébral ou d'hémorragies, des complications observées chez de nombreux patients atteints du SRAS-CoV-2 hospitalisés en USI
Prochaine étape, le développement d'assembloïdes encore plus sophistiqués comprenant non seulement des péricytes, mais également des vaisseaux sanguins capables de pomper le sang pour mieux modéliser le cerveau humain.
Des modèles qui vont permettre une meilleure compréhension du COVID-19 mais aussi des effets possibles d’autres maladies infectieuses sur le cerveau humain.
Source: Nature Medicine 09 July 2021 DOI : 10.1038/s41591-021-01443-1 A human three-dimensional neural-perivascular ‘assembloid’ promotes astrocytic development and enables modeling of SARS-CoV-2 neuropathology
Lire aussi :
